O novo medicamento para Alzheimer apresenta sinais promissores em testes
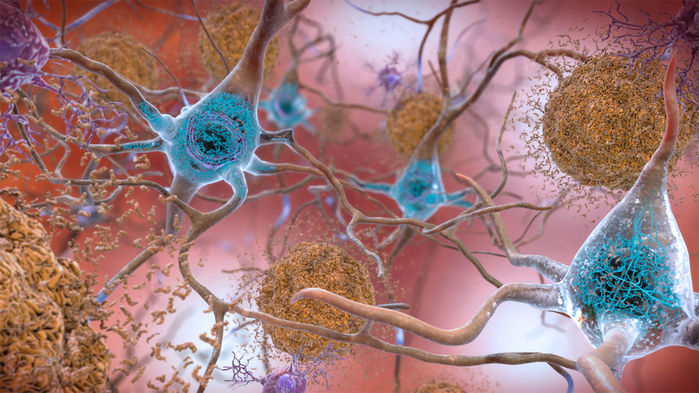
Uma nova droga de anticorpo removeu as placas de proteína (à direita) que se formam em torno dos neurônios na doença de Alzheimer. INSTITUTO NACIONAL DO ENVELHECIMENTO / INSTITUTOS NACIONAIS DE SAÚDE
Na busca por uma droga para tratar a doença de Alzheimer, até mesmo um sopro de sucesso pode ser inebriante. Isso ajuda a explicar por que uma droga experimental chamada BAN2401, que há alguns meses parecia se juntar a um crescente grupo de candidatos fracassados, gerou tanta agitação ontem na Conferência Internacional da Associação de Alzheimer em Chicago, Illinois.
Em um estudo de fase II, a droga já não mostrara o nível de benefício que seus desenvolvedores – a Biogen Inc. em Cambridge, Massachusetts; e Eisai Co. Ltd. em Tóquio – definida como o endpoint primário do estudo. Mas ontem as empresas apresentaram uma série de outras análises do mesmo estudo que sugerem que o BAN2401 pode diminuir o ritmo do declínio cognitivo nos pacientes de Alzheimer e reverter o acúmulo de uma proteína cerebral que estimula a neurodegeneração da doença. Mas o subgrupo de pacientes que mostrou esses benefícios foi relativamente pequeno – 161 pessoas – e uma mudança inesperada na forma como o estudo foi randomizado causou certo ceticismo nos resultados. Para muitos, os resultados são preliminares demais para celebrar.
“Se esses resultados que vimos hoje apresentarem-se em testes clínicos de fase III, então você está olhando para medicamentos modificadores da doença – o primeiro para a doença de Alzheimer”, diz Keith Fargo, diretor de programas científicos e divulgação da Associação de Alzheimer em Chicago. Illinois. “Mas você não sabe se eles vão dar certo até que você realmente faça o teste da fase III.”
Como vários outros medicamentos para Alzheimer em desenvolvimento, o BAN2401 tem como alvo o β-amilóide, o fragmento de proteína que forma placas pegajosas ao redor dos neurônios. Muitos cientistas acreditam que o β-amilóide é um dos principais culpados na doença de Alzheimer, bloqueando a comunicação entre os neurônios e, eventualmente, matando-os. O BAN2401 é um anticorpo que se liga e ajuda a eliminar as estruturas β-amilóides conhecidas como protofibrilas, que estão se aglomerando nas placas.
O estudo incluiu 856 pacientes com uma forma precoce e leve de Alzheimer e contou com uma nova medida de função cognitiva – o Alzheimer’s Disease Composite Score (ADCOMS) – projetado para detectar mudanças sutis em pessoas com doença em estágio inicial. As empresas também decidiram por um projeto de estudo inovador e complicado. O julgamento seria “adaptativo”; em vez de atribuir aleatoriamente um participante a um dos cinco grupos de tratamento, cada um recebendo uma dose diferente do medicamento, o sistema de atribuição aumentava a probabilidade de que um paciente recebesse a dose que parecia estar funcionando melhor no momento em que entrou no estudo. .
Os pesquisadores também se basearam em um método estatístico – conhecido como estatística bayesiana – para analisar como os diferentes grupos de pacientes estavam respondendo ao medicamento enquanto o estudo estava em andamento, em vez de esperar até que estivesse completo para fazer a análise estatística. Essa abordagem pretendia dar aos pesquisadores uma sugestão anterior sobre se a droga provavelmente funcionaria. Este foi o primeiro uso de estatísticas Bayesian em um julgamento de Alzheimer, diz Fargo. “Acho que a empresa se sentiu muito bem com essa droga”, diz ele, e acredita que a análise de Bayses pode permitir “uma decisão mais rápida sobre se deve ou não ir para a fase III”.
Mas a estratégia parece ter saído pela culatra. Essa análise inicial, com 12 meses de tratamento, deveria revelar pelo menos 80% de probabilidade de que o BAN2401 reduzisse a taxa de declínio cognitivo em 25% ou mais, em comparação com um placebo. A droga não esclareceu esse bar, Biogen e Eisai revelou em dezembro de 2017. Em vez disso, a probabilidade foi estimada em 64%, explicou Lynn Kramer, diretor clínico da divisão de neurologia de Eisai, na apresentação de ontem – “relativamente próximo”. disse.
Mas depois de seguir os pacientes por mais 6 meses, as empresas ficaram muito mais otimistas. Eles anunciaram no início deste mês que em alguns pacientes, a droga teve efeitos significativos, afinal. E a apresentação de hoje foi o primeiro vislumbre do tamanho desses efeitos: depois de 18 meses, os 161 pacientes que receberam a maior das cinco doses testadas tiveram um declínio cognitivo 30% mais lento do que os que receberam placebo, medido pelo ADCOMS. Esse grupo viu um declínio 47% mais lento do que o placebo por outra medida cognitiva mais tradicional, conhecida como subescala cognitiva da Escala de Avaliação da Doença de Alzheimer. Imagens do cérebro também revelaram que a droga reduziu os níveis de placas amilóides em todos os grupos de dosagem, e que 81% dos participantes foram considerados “negativos para amiloides” em uma tomografia cerebral após 18 meses de tratamento.
Mas Kramer também descreveu uma mudança imprevista e potencialmente problemática no julgamento. Os pesquisadores monitoraram pacientes por inchaço do cérebro, um potencial risco de segurança desse e de outros anticorpos antiamilóides – particularmente em pacientes com um gene chamado APOE4, que aumenta o risco de Alzheimer e está ligado a um declínio cognitivo mais rápido. Em julho de 2014, uma agência reguladora fora dos Estados Unidos – as empresas não especificaram qual deles – solicitou que o estudo deixasse de atribuir essas transportadoras da APOE4 ao braço de maior dose (e risco potencialmente maior) do estudo. A empresa cumpriu esse pedido.
Esse movimento não apenas reduziu o tamanho do grupo de altas doses, mas criou uma variável potencialmente confusa: esse grupo mostrou um declínio mental mais lento porque a droga estava funcionando ou porque continha menos pessoas geneticamente propensas a declinar rapidamente?
Em parte por causa dessa mudança, “acho que as pessoas provavelmente não estão tão empolgadas quanto antes”, diz Lawrence Honig, neurologista da Faculdade de Médicos e Cirurgiões Vagelos da Universidade de Colúmbia, sobre a apresentação de ontem. Ele não esteve envolvido no estudo, mas é investigador de outros estudos de drogas desenvolvidos pela Eisai e pela Biogen. A mudança para a randomização do estudo “afeta um pouco a interpretação”, diz Honig, embora “mesmo sem essas ressalvas [o teste] não seja conclusivo”. Ele observa que outros candidatos a drogas de Alzheimer pareciam promissores na fase II e falhou em um estudo maior.
Ainda não está claro que tipo de estudo a Biogen e a Eisai precisarão realizar para comprovar a eficácia do medicamento para a Food and Drug Administration dos EUA. Seu acompanhamento será um dos poucos esforços acompanhados de perto nesta classe de candidatos a medicamentos. As empresas também estão desenvolvendo em conjunto um anticorpo diferente para o alvo amiloide, o aducanumabe, que catapultou diretamente para um grande estudo de fase III em 2015, após promissoras indicações de benefício em apenas 125 pacientes. Esse estudo deverá produzir resultados em 2020.
Com informações da Science Magazine